Chương 2: Kim Loại – Hóa Học Lớp 9
Bài 18: Nhôm
Nhôm là nguyên tố phổ biến thứ ba trong vỏ Trái Đất và có nhiều ứng dụng trong đời sống và sản xuất. Nhôm có tính chất vật lí, và tính chất hóa học cùng ứng dụng quan trọng gì? Mời các bạn cùng tìm hiểu qua nội dung bài học này nhé.
- Kí hiệu hóa học: Al
- Nguyên tử khối: 27
Tóm Tắt Lý Thuyết
2. Nhôm có những tính chất hóa học của kim loại như: tác dụng với phi kim, dung dịch axit (trừ \(HNO_3\) đặc nguội, \(H_2SO_4\) đặc nguội), dung dịch muối của kim loại kém hoạt động hơn. Nhôm có phản ứng với dung dịch kiềm.
3. Nhôm và hợp kim nhôm có nhiều ứng dụng trong công nghiệp và trong đời sống.
4. Nhôm được sản xuất bằng cách điện phân hỗn hợp nóng chảy của nhôm oxit và criolit.HocTapHay.Com
I. Tính Chất Vật Lí
– Màu trắng bạc, có ánh kim.
– Kim loại nhẹ \((D = 2,7g/cm^3)\), dẻo, dẫn điện, dẫn nhiệt tốt.
– Nóng chảy ở \(660^0C\).
II. Tính Chất Hóa Học
1. Nhôm có những tính chất hóa học của kim loại không?
a. Phản ứng của nhôm với phi kim
* Phản ứng của nhôm với oxi
\(4Al (trắng) + 3O_{(2k)}(không \, \,màu) \xrightarrow{t^0} 2Al_2O_3(r)(trắng)\)
Ở điều kiện thường, nhôm phản ứng với oxi tạo thành lớp \(Al_2O_3\) mỏng bền vững. Lớp oxit naỳ bảo vệ đồ vật bằng nhôm, không cho nhôm tác dụng với oxi trong không khí và nước.
* Phản ứng của nhôm với phi kim khác
Phản ứng của nhôm với phi kim khác như \(S, Cl_2\) ,… tạo muối \(Al_2S_3, AlCl_3…\)
\(2Al_{(r)} + 3Cl_{2(k)} → 2AlCl_{3(r)}\)
Kết luận: nhôm pứ với oxi tạo thành oxit và pứ với nhiều phi kim khác như \(S, Cl_2\), … tạo muối.
b. Phản ứng của nhôm với dung dịch axit
\(2Al + 6HCl → 2AlCl_3 + 3H_2↑\)
Chú ý: Al không phản ứng với \(H_2SO_4\) đặc, nguội và \(HNO_3\) đặc, nguội.
c. Phản ứng của nhôm với dung dịch muối
\(2Al + 3CuSO_4 → Al_2(SO_4)_3 + 3Cu\)
Kết luận: nhôm phản ứng với nhiều dd muối của kim loại hoạt động hóa học yếu hơn tạo muối nhôm và giải phóng kim loại mới. Nhôm có những tính chất hóa học của kim loại.
2. Nhôm có tính chất hóa học nào khác
Nhôm phản ứng với dung dịch kiềm.
\(2Al + 2NaOH + 2H_2O → 2NaAlO_2 + 3H_2\)
III. Ứng Dụng

Ứng dụng của nhôm
Nhôm và hợp kim nhôm được sử dụng rộng rãi trong đời sống như: đồ dùng gia đình, dây dẫn điện, vật liệu xây dựng….
Đuyra (hợp kim của nhôm với đồng và một số nguyên tố khác như mangan, sắt, silic) nhẹ và bền được dùng trong công nghiệp chế tạp máy bay, ô tô. tàu vũ trụ…
IV. Sản Xuất Nhôm

Quy trình sản xuất nhôm
– Nguyên liệu: quặng bôxit (thành phần chủ yếu là \(Al_2O_3\))
– Phương pháp: điện phân nóng chảy có xúc tác Criolit
\(Al_2O_3 → 2Al + 3O_2\)
V. Tổng Kết
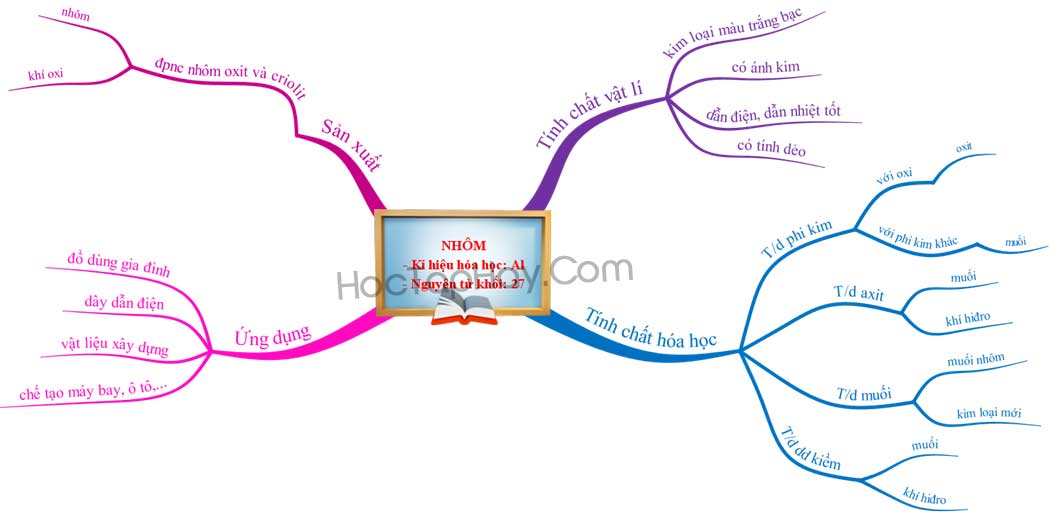
Hình sơ đồ tư duy bài nhôm
Các Bài Tập & Giải Bài Tập SGK Bài 18 Nhôm
Hướng dẫn giải bài tập sgk bài 18 nhôm chương 2 hóa học lớp 9. Bài giúp các bạn tìm hiểu về nhôm, tính chất vật lí và tính hóa học của nhôm.
Bài Tập 1 Trang 57 SGK Hóa Học Lớp 9
Hãy điền vào bảng sau những tính chất tương ứng với những ứng dụng của nhôm:
| Tính chất của nhôm | Ứng dụng của nhôm | |
| 1 | Làm dây dẫn điện | |
| 2 | Chế tạo máy bay, ô tô, xe lửa ,…. | |
| 3 | Làm dụng cụ gia đình: nồi xoong, khung cửa….. |
>> Xem: giải bài tập 1 trang 57 sgk hóa học 9
Bài Tập 2 Trang 58 SGK Hóa Học Lớp 9
Thả một mảnh nhôm vào các ống nghiệm chứa các dung dịch sau:
a. \(\)\(MgSO_4\)
b. \(CuCl_2\)
c. \(AgNO_3\)
d. \(HCl\)
Cho biết hiện tượng xảy ra. Giải thích và viết phương trình hoá học.
>> Xem: giải bài tập 2 trang 58 sgk hóa học 9
Bài Tập 3 Trang 58 SGK Hóa Học Lớp 9
Có nên dùng xô, chậu, nổi nhôm để đựng vôi, nước vôi tôi hoặc vữa xây dựng không? Hãy giải thích.
>> Xem: giải bài tập 3 trang 58 sgk hóa học 9
Bài Tập 4 Trang 58 SGK Hóa Học Lớp 9
Có dung dịch muối \(\)\(AlCl_3\) lẫn tạp chất là \(CuCl_2\). Có thể dùng chất nào sau đây để làm sạch muối nhôm? Giải thích và viết phương trình hoá học.
a. \(AgNO_3\)
b. \(HCl\)
c. \(Mg\)
d. \(Al\)
e. \(Zn\)
>> Xem: giải bài tập 4 trang 58 sgk hóa học 9
Bài Tập 5 Trang 58 SGK Hóa Học Lớp 9
Thành phần hoá học chính của đất sét là: \(\)\(Al_2O_3.2SiO_2.2H_2O\). Hãy tính phần trăm khối lượng của nhôm trong hợp chất trên.
>> Xem: giải bài tập 5 trang 58 sgk hóa học 9
Bài Tập 6 Trang 58 SGK Hóa Học Lớp 9
Để xác định thành phần phần trăm khối lượng của hỗn hợp A gồm bột nhôm và bột magie, người ta thực hiện hai thí nghiệm sau:
Thí nghiệm 1: Cho m gam hỗn hợp A tác dụng hết với dung dịch \(\)\(H_2SO_4\) loãng dư, thu được 1568 ml khí ỏ điều kiện tiêu chuẩn.
Thí nghiệm 2: Cho m gam hỗn hợp A tác dụng với dung dịch NaOH dư, sau phản ứng thấy còn lại 0,6 gam chất rắn.
Tính phần trăm khối lượng của mỗi chất trong hỗn hợp A.
>> Xem: giải bài tập 6 trang 58 sgk hóa học 9
Trên là nội dung lý thuyết bài 18 nhôm chương 2 hóa học lớp 9. Hi vọng bài học giúp các bạn tìm hiểu được nhôm và biết được ứng dụng cuả nhôm trong đời sống. Bạn thấy nội dung bài học này thế nào? Để lại ý kiến đóng góp ngay bên dưới đây nhé.
Bài Tập Liên Quan:
- Bài 24: Ôn Tập Học Kì I
- Bài 23: Thực Hành Tính Chất Hóa Học Của Nhôm Và Sắt
- Bài 22: Luyện Tập Chương 2 Kim Loại
- Bài 21: Sự Ăn Mòn Kim Loại Và Bảo Vệ Kim Loại Không Bị Ăn Mòn
- Bài 20: Hợp Kim Sắt Gang, Thép
- Bài 19: Sắt
- Bài 17: Dãy Hoạt Động Hóa Học Của Kim Loại
- Bài 16: Tính Chất Hóa Học Của Kim Loại
- Bài 15: Tính Chất Vật Lí Của Kim Loại
Trả lời