Chương 3: Phi Kim. Sơ Lược Về Bảng Tuần Hoàn Các Nguyên Tố Hóa Học – Hóa Học Lớp 9
Bài 31: Sơ Lược Về Bảng Tuần Hoàn Các Nguyên Tố Hóa Học
Bảng tuần hoàn của các nguyên tố hóa học được cấu tạo như thế nào và có ý nghĩa gì? Mời các bạn cùng đi tìm hiểu nội dung bài 31 sơ lược về bảng tuần hoàn các nguyên tố hóa học.
Tóm Tắt Lý Thuyết
2. Cấu tạo bảng tuần hoàn gồm có ô nguyên tố, chu kì, nhóm.
3. Sự biến đổi tính chất của các nguyên tố trong chu kì (2, 3) và nhom (I, VII).
4. Ý nghĩa của bảng tuần hoàn
– Biết vị trí suy ra cấu tạo nguyên tử và tính chất của nguyên tố.
– Biết cấu tạo nguyên tử, suy ra vị trí và tính chất của nguyên tố.HocTapHay.Com
I. Nguyên Tắc Sắp Xếp Các Nguyên Tố Trong Bảng Tuần Hoàn
Trong bảng tuần hoàn, các nguyên tố được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử.
Cách khác: Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn, sắp xếp các nguyên tố theo chiều tăng dần của số điện tích hạt nhân.
II. Cấu Tạo Bảng Tuần Hoàn
1. Ô nguyên tố
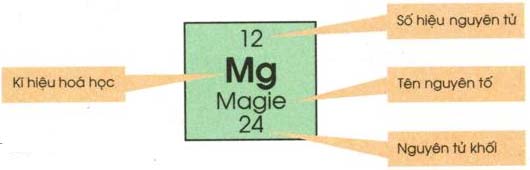
Ô nguyên tố
Bảng tuần toàn có khoảng 110 ô, mỗi ô xếp một nguyên tố.
– Ô nguyên tố cho biết: Số hiệu nguyên tử, kí hiệu hóa học, tên nguyên tố, nguyên tử khối của nguyên tố đó.
– Số hiệu nguyên tử là số thứ tự của nguyên tố trong bảng hệ thống tuần hoàn. Số hiệu nguyên tử có trị số bằng số đơn vị điện tích hạt nhân và bằng số electron trong nguyên tử.
Ví du: ô thứ 11, xếp nguyên tố natri (Na). Ta có:
– Số nguyên tử = số proton = số electron = 11
– Kí hiệu hóa học: Na
– Tên nguyên tố: Natri
– Nguyên tử khối: 23
2. Chu kì
Chu kì gồm các nguyên tố mà nguyên tử của chúng có thể cùng số lớp electron và được xếp thành hàng theo chiều tăng dần điện tích hạt nhân.
– Số thứ tự của chu kì bằng số lớp electron trong nguyên tử của các nguyên tố nằm trong chu kì.
Ví dụ: Chu kì II, tất cả các nguyên tử đều có 2 lớp electron.
– Trong bảng tuần hoàn gồm 7 chu kì (mỗi chi kì là một hàng).
– Trừ chu kì I, các chu kì còn lại đều bắt đầu là kim loại kiềm và kết thúc là khí hiếm.
Ví dụ: chu kì 3: bắt đầu là kim loại kiềm Na và kết thúc là khí trơ: Ar (agon)
3. Nhóm
– Nhóm gồm các nguyên tố mà nguyên tử của chúng có số electron lớp ngoài cùng bằng nhau, do đó có tính chât tương tự nhau.
– Mỗi nhóm được xếp thành một cột theo chiều tăng của điện tích hạt nhân. Bảng tuần hoàn có 8 nhóm A và 8 nhóm B. Nhóm IA (trừ H) là các kim loại mạnh, gọi là các kim loại kiềm; Nhóm VIIA là các phi kim mạnh, gọi là nhóm halogen; Nhóm VIIIA là các khí hiếm (hay khí trơ).
– Số thứ tự của các nhóm A bằng số electrdn ở lớp ngoài cùng của nguyên tử trong nhóm đó.
III. Sự Biến Đổi Tính Chất Của Các Nguyên Tố Trong Bảng Tuần Hoàn
1. Trong một chu kì
Khi đi từ đầu chu kì đến cuối chi kì theo chiều tăng dần điện tích hạt nhân, ta có:
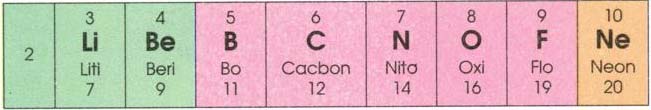
– Số electron ngoài cùng của nguyên tử tăng dần tứ 1 đến 8 (trừ chu kì 1).
– Tính kim loại của nguyên tố giảm dần, đồng thời tính phi kim tăng dần. Có nghĩa đầu chi kì là kim lọai mạnh (kim loại kiềm), cuối chi kì là phi kim mạnh (halogen: flo, clo…), kết thúc chu kì là khí hiếm.
Ví dụ: chu kì 3 là kim loại kiềm Na (kim loại mạnh), cuối chu kì là phi kim mạnh clo, kết thúc chu kì là khí hiếm agon (Ar).

2. Trong một nhóm
Khi đi từ trên xuống theo chiều tăng điện tích hạt nhân, ta có: số lớp electron của nguyên tử tăng dần, tính kim loại của các nguyên tố tăng dần, đồng thời tính phi kim giảm dần.
IV. Ý Nghĩa Bảng Tuần Hoàn Các Nguyên Tố Hóa Học
a. Biết vị trí của nguyên tố ta có thể suy đoán cấu tạo nguyên tử và tính chất của nguyên tố.
Thí dụ: Nguyên tố A có số hiệu nguyên tử là 17, chu kì 3, nhóm VIIA. Hãy cho biết cấu tạo nguyên tử, tính chất nguyên tử A và so sánh với các nguyên tố bên cạnh.
Giải: Số hiệu nguyên tử là 17, suy ra điện tích hạt nhân của nguyên tử A là 17+, nguyên tử A có 17 electron.
– Ở chu kì 3, suy ra nguyên tử A có 3 lớp electron; nhóm VIIA suy ra lớp ngoài cùng có 7e.
– Nguyên tố A (Cl) ở cuối chu kì 3 nên là một phi kim mạnh, tính phi kim của A mạnh hơn của nguyên tố trước nó trong cùng chu kì (là s có số hiệu là 16) và nguyên tố đứng dưới nó trong cùng nhóm (là Br có số hiệu nguyên tử là 35) nhưng kém nguyên tố phía trên nó trong cùng nhóm (là F có số hiệu nguyên tử là 9)
b. Biết cấu tạo nguyên tử của nguyên tố có thể suy đoán vị trí và tính chất nguyên tố đó.
Thí dụ: Nguyên tố X có điện tích hạt nhân là 11+, 3 lớp electron, lớp ngoài cùng có 1 electron.
Hãy cho biết vị trí của X trong bảng tuần hoàn và tính chất cơ bản của nó.
Giải:
– Vì nguyên tử X có điện tích hạt nhân là 11+, 3 lớp electron và có le ở lớp ngoài cùng, suy ra nguyên tố X ở ô 11, chu kì 3, nhóm IA
– Nguyên tố A ở đầu chu kì nên tính chất hóa học cơ bản là tính kim loại. Ngoài ra, bảng tuần hoàn các nguyên tố hóa học là cơ sở khoa học quan trọng giúp ta có phương pháp học tập, nghiên cứu hóa học một cách có hệ thống.
Các Bài Tập & Lời Giải Bài Tập SGK Bài 31 Sơ Lược Về Bảng Tuần Hoàn Các Nguyên Tố Hóa Học
Hướng dẫn làm các bài tập sgk bài 31 sơ lược về bảng tuần hoàn các nguyên tố hóa học chương 3. Nội dung bài học giúp các bạn tìm hiểu các khái niệm về bảng tuần hoàn và giải các bài tập sgk.
Bài Tập 1 Trang 101 SGK Hóa Học Lớp 9
Dựa vào bảng tuần hoàn, hãy cho biết cấu tạo nguyên tử, tính chất kim loại, phi kim của các nguyên tố có số hiệu nguyên tử 7, 12, 16.
>> Xem: giải bài tập 1 trang 101 sgk hóa học lớp 9
Bài Tập 2 Trang 101 SGK Hóa Học Lớp 9
Biết X có cấu tạo nguyên tử như sau: điện tích hạt nhân là 11+, 3 lớp electron, lớp ngoài cùng có 1 electron. Hãy suy ra vị trí của X trong bảng tuần hoàn và tính chất hoá học cơ bản của nó.
>> Xem: giải bài tập 2 trang 101 sgk hóa học lớp 9
Bài Tập 3 Trang 101 SGK Hóa Học Lớp 9
Các nguyên tố trong nhóm I đều là những kim loại mạnh tương tự natri: tác dụng với nước tạo thành dung dịch kiềm và giải phóng hiđro, tác dụng với oxi tạo thành oxit, tác dụng với phi kim khác tạo thành muối … Viết các phương trình hoá học minh hoạ với kali.
>> Xem: giải bài tập 3 trang 101 sgk hóa học lớp 9
Bài Tập 4 Trang 101 SGK Hóa Học Lớp 9
Các nguyên tố nhóm VII đều là những phi kim mạnh tương tự clo (trừ At): tác dụng với hầu hết kim loại tạo muối, tác dụng với hiđro tạo hợp chất khí. Viết phương trình hoá học minh hoạ với brom.
>> Xem: giải bài tập 4 trang 101 sgk hóa học lớp 9
Bài Tập 5 Trang 101 SGK Hóa Học Lớp 9
Hãy cho biết cách sắp xếp nào sau đây đúng theo chiều tính kim loại giảm dần:
a. Na, Mg, Al, K
b. K, Na, Mg, Al
c. Al, K, Na, Mg
d. Mg, K, Al, Na.
Giải thích sự lựa chọn.
>> Xem: giải bài tập 5 trang 101 sgk hóa học lớp 9
Bài Tập 6 Trang 101 SGK Hóa Học Lớp 9
Hãy sắp xếp các nguyên tố sau theo chiều tính phi kim tăng dần : F, O, N, P, As.
>> Xem: giải bài tập 6 trang 101 sgk hóa học lớp 9
Bài Tập 7 Trang 101 SGK Hóa Học Lớp 9
a. Hãy xác định công thức của hợp chất khí A, biết rằng:
– A là oxit của lưu huỳnh chứa 50% oxi.
– 1 gam khí A chiếm thề tích là 0,35 lít ở đktc.
b. Hoà tan 12,8 gam hợp chất khí A vào 300 ml dung dịch NaOH 1,2M. Hãy cho biết muối nào thu được sau phản ứng. Tính nồng độ mol của muối (giả thiết thể tích dung dịch thay đổi không đáng kể).
>> Xem: giải bài tập 7 trang 101 sgk hóa học lớp 9
Em Có Biết?
Dựa vào bảng tuần hoàn, Men-đê-lê-ép đã dư đoán tính chất của một số nguyên tố chưa biết. Thí dụ như đối với nguyên tố gemani (Ge).
| Tính chất do Men-đê-lê-ép dự đoán | Tính chất xác định được | |
| Nguyên tử khối | 72 | 72,6 |
| Khối lượng riêng | \(\)\(5,5g/cm^3\) | \(5,3 g/cm^3\) |
| Tính chất, màu sắc | Kim loại, màu tối | Kim loại, màu xám |
| Điểm nóng chảy | Điểm nóng chảy cao | \(937^0C\) |
Các bạn vừa xem lý thuyết nội dung bài 31 sơ lược về bảng tuần hoàn các nguyên tố hóa học chương 3 hóa học lớp 9. Hi vọng bài học sẽ giúp các bạn hiểu rõ hơn về bảng tuần hoàn các nguyên tố hóa học, bạn thấy bài viết này thế nào? Để lại ý kiến đóng góp ngay bên dưới nhé. Chúc các bạn học tốt hóa học 9.
Bài Tập Liên Quan:
- Bài 33: Thực Hành Tính Chất Hóa Học Của Phi Kim Và Hợp Chất Của Chúng
- Bài 32: Luyện Tập Chương 3: Phi Kim – Sơ Lược Về Bảng Tuần Hoàn Các Nguyên Tố Hoá Học
- Bài 30: Silic. Công Nghiệp Silicat
- Bài 29: Axit Cacbonic Và Muối Cacbonat
- Bài 28: Các Oxit Của Cacbon
- Bài 27: Cacbon
- Bài 26: Clo
- Bài 25: Tính Chất Của Phi Kim
Trả lời