Chương 4: Hiđrocacbon. Nhiên Liệu – Hóa Học Lớp 9
Bài 37: Etilen
Etilen là nguyên liệu để điều chế polietilen, được dùng trong công nghiệp chất dẻo. Qua bài học này sẽ giúp các bạn tìm hiểu công thức cấu tạo, tính chất và ứng dụng của etilen nhé.
- Công thức phân tử: \(C_2H_4\)
- Phân tử khối: 28
Tóm Tắt Lý Thuyết
2. Công thức cấu tạo của etilen là \(CH_2=CH_2\)
3. Etilen có các tính chất hóa học sau: tham gia phản ứng cháy, phản ứng cộng và phản ứng trùng hợp.
4. Etilen là nguyên liệu để điều chế nhựa polime, rượu etylic, axit axetic….HocTapHay.Com
I. Tính Chất Vật Lí
– Trạng thái: khí
– Màu sắc: không màu
– Khả năng tan trong nước: ít tan
– \(d_{C_2H_4/ KK} = 28/29\) nhẹ hơn không khí.
II. Cấu Tạo Phân Tử
– CTPT: C_2H_4
– CTCT: 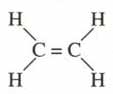
– CTCT: (thu gọn): \(CH_2 = CH_2\)
- Giữa hai nguyên tử C có hai liên kết, những liên kết như vậy gọi là liên kết đôi
- Trong liên kết đôi có một liên kết kém bền.Liên kết này dễ bị đứt ra trong các phản ứng hóa học.
Chú ý: Trong phân tử có 1 liên kết đôi
+ 1 liên kết đơn bền
+ 1 liên kết kém bền, dễ bị cắt đứt để tham gia liên kết với nguyên tử khác.
Phân tử có 4 liên kết đơn C-H và một liên kết đôi C = C. Trong liên kết đôi có một liên kết kém bền, dễ bị đứt ra trong các phản ứng hoá học.
Một số hợp chất trong CTCT có 1 liên kết đôi như \(CH_2 = CH_2\) có dạng tổng quát: \(C_nH_{2n} (n ≥ 2)\)
– Etilen: có một liên kết đôi và 4 liên kết đơn, các nguyên tử cùng nằm trên một mặt phẳng.
– Metan: không có liên kết đôi, các nguyên tử H nằm ở đỉnh và C nằm ở tâm của hình tứ diện đều.

Mô hình phân tử Etilen
a) Mô hình rỗng b) Mô hình đặc
III. Tính Chất Hóa Học
1. Etilen có cháy không?
\(C_2H_4 + 3O_2 \xrightarrow{t^0} 2CO_2↑ + 2H_2O\)
Dạng tổng quát:
\(C_nH_{2n} + (3n/2)O_2 \xrightarrow{t^0} nCO_2↑ + nH_2O\)
2. Etilen có làm mất màu dung dịch brom không?

Thí nghiệm etilen tác dụng với dung dịch nước Brom
a. Dung dịch Brom
\(CH_2 = CH_2 + Br-Br → CH_2=CH_2\) (đibrometan)
PTHH viết gọn:
\(C_2H_4 + Br_2 → C_2H_4Br_2\)
Tổng quát: \(C_nH_2 n + Br_2 → CnH_2nBr_2\)
Etilen làm mất màu dung dịch brom → cách nhận etilen
b. Cộng hiđro
\(CH_2=CH_2 + H – H \xrightarrow{Ni, t^0} CH_3 – CH_3\)
Tổng quát: \(C_nH_{2n} + H_2 \xrightarrow{Ni, t^0} C_nH_{2n+2}\)
c. Cộng axit:
\(CH_2=CH_2 + HCl → CH_3–CH_2-Cl\) (Etyl Clorua)
Dạng tổng quát: \(C_nH_{2n} + HX → C_nH_{2n+1}X\)
d. Cộng nước:
\(CH_2=CH_2 + H-OH \xrightarrow{H_2SO_4, t^0} CH_3-CH_2-OH\) (Rượu Etylic)
3. Các phân tử etilen có kết hợp được với nhau không?
Điều kiện: nhiệt độ cao, áp suất cao, chất xúc tác thích hợp.
\(n_{CH_2} = CH_2 \xrightarrow{P, xt, t^0} [CH_2=CH_2]_n\)
Etilen Poly Etilen
Chú ý: Chỉ có C mang liên kết đôi mới tham gia mở nối trùng hợp.
Trùng hợp là quá trình cộng hợp liên tiếp nhiều monome ( phân tử nhỏ ) giống nhau hoặc tương tự nhau thành polyme ( phân tử rất lớn )
IV. Ứng Dụng Etilen
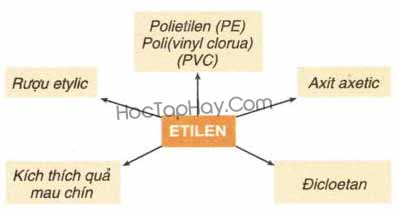
Ứng dụng của etilen
– Tổng hợp Polime : PE, PP, PVC…
– Tổng hợp các hóa chất khác: etanol, etilen oxit, etylen glicol …
V. Tổng Kết Etilen

Hình: Sơ đồ tư duy bài Etilen
Các Bài Tập & Lời Giải Bài Tập SGK Bài 37 Etilen
Hướng dẫn các bạn hoàn thành các bài tập sgk bài 37 Etilen chương 4 hóa học lớp 9. Nội dung giúp các bạn tìm hiểu công thức cấu tạo, tính chất và ứng dụng của etilen.
Bài Tập 1 Trang 119 SGK Hóa Học Lớp 9
Hãy tính số liên kết đơn, liên kết đôi giữa những nguyên tử cacbon trong phân tử các chất sau:
a. \(\)\(CH_3 – CH_3\)
b. \(CH_2 = CH_2\)
c. \(CH_2 = CH – CH = CH_2\).
>> Xem: giải bài tập 1 trang 119 sgk hóa học lớp 9
Bài Tập 2 Trang 119 SGK Hóa Học Lớp 9
Điền từ thích hợp “có” hoặc “không” vào các cột sau:
| Có liên kết đôi | Làm mất màu dung dịch brom | Phản ứng trùng hợp | Tác dụng với oxi | |
| Metan | ||||
| Etilen |
>> Xem: giải bài tập 2 trang 119 sgk hóa học lớp 9
Bài Tập 3 Trang 119 SGK Hóa Học Lớp 9
Hãy nêu phương pháp hoá học loại bỏ khí etilen có lẫn trong khí metan để thu đuợc metan tinh khiết.
>> Xem: giải bài tập 3 trang 119 sgk hóa học lớp 9
Bài Tập 4 Trang 119 SGK Hóa Học Lớp 9
Để đốt cháy 4,48 lít khí etilen cần phải dùng:
a. Bao nhiêu lít oxi?
b. Bao nhiêu lít không khí chứa 20% thể tích oxi?
Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
>> Xem: giải bài tập 4 trang 119 sgk hóa học lớp 9
Em Có Biết?
Cách làm quả mau chín:
Từ lâu, người ta đã biết khi xếp một số quả chính vào giữa quả xanh thì toàn bộ quả xanh sẽ nhanh chóng chín đều. Tại sao vậy?
Bí mật của hiện tượng này đã được các nhà khoa học phát hiện khi nghiên cứu quá trình chín của trái cây. Trong quá trình chín trái cây đã thoát ra một lượng nhỏ khí etilen. Khí etilen sinh ra có tác dụng xúc tác quá trình hô hấp của tế bào trái cây và làm cho quả mau chín.
Nắm được bí quyết đó, người ta có thể làm chậm quá trình chín của trái cây bằng cách làm giảm nồng độ etilen do trái cây sinh ra. Điều này đã được sử dụng để bảo quản trái cây không bị chín nẫu khi vận chuyển xa. Ngược lại, khi cần cho quả mau chín, người ta thêm etilen vào kích thích quá trình hô hấp của tế bào trái cây.
Như vậy, các bạn vừa hoàn thành nội dung lý thuyết bai 37 etilen chương 4 hóa học 9. Bài học giúp bạn tìm hiểu công thức cấu tạo, tính chất vật lí và ứng dụng của etilen. Qua bài học này bạn rút ra được điều gì? để lại ý kiến đóng góp ngay bên dưới nhé.
Trả lời