Chương 6: Dung Dịch – Hóa Học Lớp 8
Bài 41: Độ Tan Của Một Chất Trong Nước
Nội dung bài học bài 41 độ tan của một chất trong nước chương 6 hóa học lớp 8. Bài học giúp các bạn hiểu được khái niệm về chất tan và không tan, biết được tính tan của một số axit, bazơ, muối trong nước. Hiểu được khái niệm độ tan của một chất trong nước và các yếu tố ảnh hưởng đến độ tan.
Các em đã biết, ở một nhiệt độ nhất định các chất khác nhau có thể bị hòa tan nhiều hay ít khác nhau. Đối với một chất nhất định, ở những nhiệt độ khác nhau cũng hòa tan nhiều ít khác nhau. Để có thể xác định được lượng chất tan này, chúng ta hãy tìm hiểu độ tan của chất.
Độ tan của một chất trong nước:
Độ tan (S) của một chất là số gam chất đó tan được trong 100 gam nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định.
Nói chung độ tan của chất rắn sẽ tăng nếu tăng nhiệt độ. Độ tan của chất khí sẽ tăng nếu giảm nhiệt độ và tăng áp suất.
HocTapHay.ComI. Chất Tan Và Chất Không Tan
1. Thí nghiệm về tính tan của chất
Thí nghiệm 1:
Lấy một lượng nhỏ canxi cacbonat sạch \((CaCO_3)\) cho vào nước cất, lắc mạnh. Lọc lấy nước lọc. Nhỏ vài giọt nước lọc trên tấm kính sạch. Làm bay hơi nước từ từ cho đến hết (hình 6.4).
Quan sát: Sau khi bay hơi nước, trên tấm kính không để lại dấu vết.
Kết luận: Canxi cacbonat không tan trong nước.
Thí nghiệm 2:
Thay muối canxi cacbonat bằng muối ăn (NaCl) rồi làm thí nghiệm như trên (hình 6.4).

Hình 6.4
Quan sát: Sau khi bay hết hơi nước, trên tấm kính có vết mờ.
Kết luận: Natri clorua tan được trong nước.
Ta nhận thấy, có chất không tan và có chất tan trong nước. Có chất tan nhiều và có chất tan ít trong nước.
2. Tính tan trong nước của một số axit, bazơ, muối
Axit: Hầu hết axit tan được trong nước, trừ axit silixic \((H_2SiO_3)\)
Bazơ: Phần lớn các bazơ không tan trong nước, trừ một số như: \(KOH, NaOH, Ba(OH)_2\), còn \(Ca(OH)_2\) ít tan.
Muối:
a. Những muối natri, kali đều tan
b. Những muối nitrat đều tan
c. Phần lớn các muối clorua, sunfat tan được. Nhưng phần lớn muối cacbonat không tan.

II. Độ Tan Của Một Chất Trong Nước
Để biểu thị khối lượng chất tan trong một khối lượng dung môi, người ta dùng “độ tan”.
1. Định nghĩa
Độ tan (kí hiệu là S) của một chất trong nước là số gam chất đó hòa tan trong 100 gam nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định.
Thí dụ: ở \(25^0C\) độ tan của đường là 204g, của NaCl là 36g, của \(AgNO_3\) là 222g..
2. Những yếu tố ảnh hưởng đến độ tan
a. Độ tan của chất rắn trong nước phụ thuộc vào nhiệt độ. Trong nhiều trường hợp, khi tăng nhiệt độ thì độ tan của chất rắn cũng tăng theo. Số ít trường hợp, khi tăng nhiệt độ thì độ tan lại giảm (hình 6.5).

Hình 6.5: Ảnh hưởng của nhiệt độ đến độ tan của chất rắn
b. Độ tan của chất khí trong nước phụ thuộc vào nhiệt độ và áp suất. Độ tan chất khí trong nước sẽ tăng, nếu ta giảm nhiệt độ (hình 6.6) và tăng áp suất.
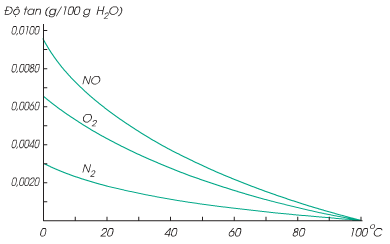
Hình 6.6: Ảnh hưởng của nhiệt độ đến độ tan của chất khí
Kiến Thức Trọng Tâm
1. Tính tan của các hợp chất trong nước:
Bazơ: phần lớn các bazơ không tan, trừ \(NaOH, KOH, Ba(OH)_2\).
Axit: hầu hết các axit tan được, trừ \(H_2SiO_3\).
Muối: Các muối nitrat đều tan.
Phần lớn các muối clorua và sunfat tan được, trừ \(AgCl, PbSO_4, BaSO_4\).
Phần lớn muối cacbonat không tan trừ \(Na_2CO_3, K_2CO_3\).
2. Độ tan của một chất trong nước:
Độ tan (S) của một chất là số gam chất đó tan được trong 100g nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định.
Độ tan của chất rắn sẽ tăng, nếu tăng nhiệt độ. Độ tan của chất khí sẽ tăng, nếu giảm nhiệt độ và tăng áp suất.
Bài Tập
Bài Tập 1 Trang 142 SGK Hóa Học Lớp 8
Hãy chọn câu trả lời đúng.
Độ tan của một chất trong nước ở nhiệt độ xác định là:
A. Số gam chất đó có thể tan trong 100 gam dung dịch
B. Số gam chất đó có thể tan trong 100 gam nước.
C. Số gam chất đó có thể tan trong 100 gam dung môi để tạo thành dung dịch bão hòa.
D. Số gam chất đó có thể tan trong 100 gam nước để tạo thành dung dịch bão hòa.
Bài Tập 2 Trang 142 SGK Hóa Học Lớp 8
Khi tăng nhiệt độ thì độ tan của các chất rắn trong nước:
A. Đều tăng
B. Đều giảm;
C. Phần lớn là tăng
D. Phần lớn là giảm;
E. Không tăng và cũng không giảm.
Bài Tập 3 Trang 142 SGK Hóa Học Lớp 8
Khi giảm nhiệt độ và tăng áp suất thì độ tan của chất khí trong nước:
A. Đều tăng
B. Đều giảm
C. Có thể tăng và có thể giảm
D. Không tăng và cũng không giảm.
Bài Tập 4 Trang 142 SGK Hóa Học Lớp 8
Dựa vào đồ thị về độ tan của các chất rắn trong nước (hình 6.5), hãy cho biết độ tan của các muối \(\)\(NaNO_3, KBr, KNO_3, NH_4Cl, NaCl, Na_2SO_4\) ở nhiệt độ \(10^0C\) và \(60^0C\).
Bài Tập 5 Trang 142 SGK Hóa Học Lớp 8
Xác định độ tan của muối \(\)\(Na_2CO_3\) trong nước ở \(18^0C\). Biết rằng ở nhiệt độ này khi hòa tan hết 53g \(Na_2CO_3\) trong 250g nước thì được dung dịch bão hòa.
Trên là toàn bộ lý thuyết và nội dung bài 41 độ tan của một chất trong nước chương 6 dung dịch. Bài học giúp bạn rèn kĩ năng quan sát thí nghiệm, từ thí nghiệm rút ra nhận xét, kĩ năng làm một số bài toán có liên quan đến độ tan.
Trả lời