Chương 1: Các Loại Hợp Chất Vô Cơ – Hóa Học Lớp 9
Bài 9: Tính Chất Hóa Học Của Muối
Muối rất quen thuộc với đời sống của chúng ta. Vậy muối có những tính chất hóa học nào? Và thế nào là phản ứng tra đổi? Điều kiện xảy ra phản ứng trao đổi là gì? Mời các bạn tham khảo nội dung bài 9 tính chất hóa học của muối.
Tóm Tắt Lý Thuyết
2. Phản ứng trao đổi là phản ứng hóa học, trong đó hai hợp chất tham gia phản ứng trao đổi với nhau những thành phần cấu tạo của chúng để tạo ra những hợp chất mới không tan hoặc chất khí.HocTapHay.Com
I. Tính Chất Hóa Học Của Muối
1. Muối tác dụng với kim loại
\(Cu(r) + AgNO3(dd) → Cu(NO_3)_2 (dd) + Ag(r)↓\)
* Điều kiện:
– Kim loại tác dụng phải đứng trước kim loại trong dung dịch muối.
– Muối mới phải tan.
Hiện tượng: Có kim loại màu xám bạc bám bên ngoài dây đồng. Dung dịch ban đầu không màu dần chuyển qua màu xanh.
Giải thích: Do xảy ra phản ứng \(Cu+ AgNO_3 → Cu(NO_3)_2 + 2Ag\). Kim loại Ag sinh ra, bám vào dây đồng và dung dịch có màu xanh của \(Cu(NO_3)_2\)
2. Muối tác dụng với axit
\(BaCl_{2}(dd) + H_2O_4(dd) → BaSO_4(r) + 2HCl(dd)\)
* Điều kiện: muối mới phải kết tủa hoặc axit mới tạo chất dể bay hơi.
Hiện tượng: Có kết tủa trắng xuất hiện
Giải thích: Gốc bằng \(SO_4\) trong phân tử \(H_2SO_4\) kết hợp với nguyên tố Bari trong phân tử \(BaCl_2\) tạo thành kết tủa \(BaSO_4\)
Phương trình hóa học: \(H_2SO_4 + BaCl_2 → BaSO_4 + 2HCl\)
3. Muối tác dụng với muối
\(NaCl (dd) + AgNO_3(dd) → NaNO_3(dd) + AgCl(r)\)
* Điều kiện: Sau phản ứng phải có ít nhất 1 muối không tan (kết tủa).
Hiện tượng: Xuất hiện kết tủa trắng
Giải thích: Do xảy ra phản ứng \(AgNO_3 + NaCl → AgCl + NaNO_3\). Kết tủa trắng chính là AgCl sỉnh ra.
4. Muối tác dụng với Bazơ (tạo Muối mới + bazơ mới)
\(CuSO_4(dd) + 2NaOH(dd) → Cu(OH)_2(r) + Na_2SO_4(dd)\)
\(Na_2CO_3(dd) + Ba(OH)_2(dd) → 2NaOH + BaCO_3(r)\)
Điều kiện: Sau phản ứng phải có ít nhất 1 muối không tan
5. Phản ứng phân hủy muối
\(2KClO_3 → 3KCl + 3O_2↑\)
\(CaCO_3 → CaO + CO_2↑\)
II. Phản Ứng Trao Đổi Trong Dung Dịch
1. Nhận xét về các phản ứng hóa học của muối
\(BaCl_2(dd) + Na_2SO_4 (dd) → BaSO_4 (r) + 2NaCl (dd)\)
\(CuSO_4 (dd) + 2NaOH (dd) → Cu(OH)_2(r) + Na_2SO_4 (dd)\)
\(Na_2CO_3 (dd) + H_2SO_4 (dd) → Na_2SO_4 (dd) + CO_2 (k) + H_2O(l)\)
Trong các phản ứng hóa học của muối, luôn có sự trao đổi thành phần với nhau để tạo ra hợp chất mới.
2. Phản ứng
Phản ứng trao đổi là phản ứng hóa học trong đó 2 hợp chất tham gia phản ứng trao đổi với nhau những thành phần cấu tạo của chúng để tạo ra những hợp chất mới.
3. Điều kiện xảy ra phản ứng
Điều kiện xaỷ ra phản ứng trao đổi là phản ứng trao đổi trong dung dịch các chất chỉ xảy ra khi sản phẩm tạo thành có chất không tan hoặc chất khí.
III. Tổng Kết
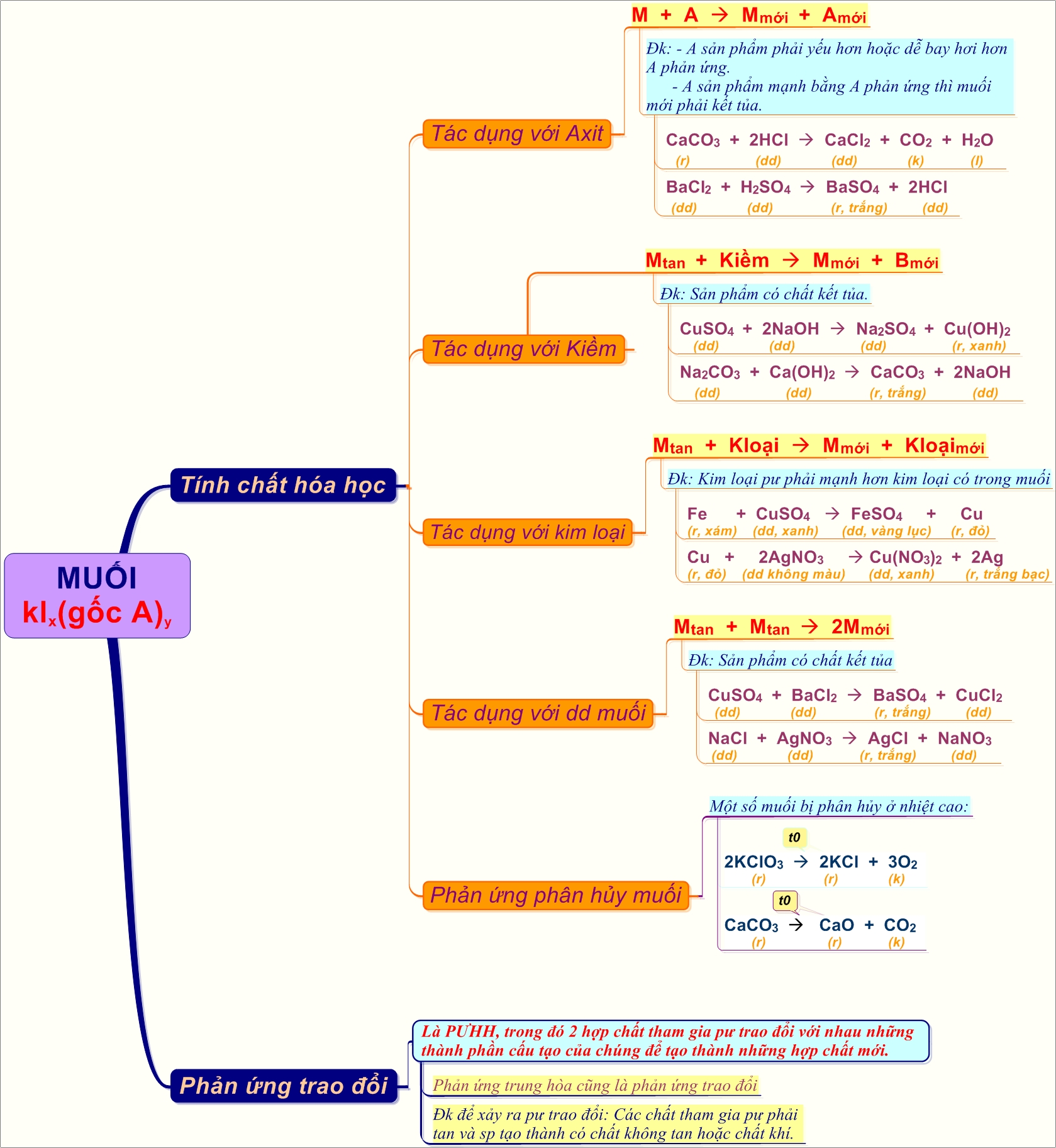
Hình: Sơ đồ tư duy bài tính chất hóa học của muối
Các Bài Tập & Lời Giải Bài Tập SGK Bài 9 Tính Chất Hóa Học Của Muối
Hướng dẫn giải bài tập sgk bài 9 tính chất hóa họ của muối chương 1 hóa học 9. Bài giúp các bạn tìm hiểu tính chất hóa học của muối và phản ứng trao đổi dung dịch của muối, áp dụng kiến thức giải các bài tập sgk.
Bài Tập 1 Trang 33 SGK Hóa Học Lớp 9
Hãy dẫn ra một dung dịch muối khi tác dụng với một dung dịch chất khác thì tạo ra:
a. Chất khí
b. Chất kết tủa.
Viết phương trình hóa học.
Xem: giải bài tập 1 trang 33 sgk hóa học lớp 9
Bài Tập 2 Trang 33 SGK Hóa Học Lớp 9
Có 3 lọ không nhãn, mỗi lọ đựng một dung dịch muối: \(\)\(CuSO_4, AgNO_3, NaCl\). Hãy dùng những dung dịch có sẵn trong phòng thí nghiệm để nhận biết chất đựng trong mỗi lọ. Viết các phương trình hóa học.
Xem: giải bài tập 2 trang 33 sgk hóa học lớp 9
Bài Tập 3 Trang 33 SGK Hóa Học Lớp 9
Có những dung dịch muối sau: \(\)\(Mg(NO_3)_2, CuCl_2\). Hãy cho biết muối nào có thể tác dụng với:
a. Dung dịch NaOH
b. Dung dịch HCl
c. Dung dịch \(AgNO_3\)
Nếu có phản ứng, hãy viết các phương trình hóa học.
Xem: giải bài tập 3 trang 33 sgk hóa học lớp 9
Bài Tập 4 Trang 33 SGK Hóa Học Lớp 9
Cho những dung dịch muối sau đây phản ứng với nhau từng đôi một, hãy ghi dấu (x) nếu có phản ứng, dấu (o) nếu không.
| \(Na_2CO_3\) | \(KCl\) | \(Na_2SO_4\) | \(NaNO_3\) | |
| \(Pb(NO_3)_2\) | ||||
| \(BaCl_2\) |
Viết phương trình hóa học ở ô có dấu (x).
Xem: giải bài tập 4 trang 33 sgk hóa học lớp 9
Bài Tập 5 Trang 33 SGK Hóa Học Lớp 9
Ngâm một đinh sắt sạch trong dung dịch (II) sunfat. Câu trả lời nào sau đây là đúng nhất cho hiện tượng quan sát được?
a. Không có hiện tượng nào xảy ra.
b. Kim loại đồng màu đỏ bám ngoài đinh sắt, đinh sắt không có sự thay đổi.
c. Một phần đinh sắt bị hòa tan, kim loại đồng bám ngoài đinh sắt và màu xanh lam của dung dịch ban đầu nhạt dần.
d. Không có chất mới nào được sinh ra, chỉ có một phần đinh sắt bị hòa tan.
Giải thích cho sự lựa chọn và viết phương trình hóa học nếu có.
Xem: giải bài tập 5 trang 33 sgk hóa học lớp 9
Bài Tập 6 Trang 33 SGK Hóa Học Lớp 9
Trộn 30 ml dung dịch có chứa 2,22g \(\)\(CaCl_2\) với 70 ml dung dịch có chứa \(AgNO_3\).
a. Hãy cho biết hiện tượng quan sát được và viết phương trình hóa học.
b. Tính khối lượng chất rắn sinh ra.
c. Tính nồng độ mol của chất còn lại trong dung dịch sau phản ứng. Cho rằng thể tích của dung dịch thay đổi không đáng kể.
Xem: giải bài tập 6 trang 33 sgk hóa học lớp 9
Trên là toàn bộ nội dung bài 9 tính chất hóa học của muối chương 1 hóa học 9. Bài học giúp các bạn tìm hiểu về tính chất hóa học muối và phản ứng trao đổi dung dịch muối. Bạn thấy nội dung bài học này thế nào, để lại ý kiến ngay bên dưới nhé.
Bài Tập Liên Quan:
- Bài 14: Thực Hành Tính Chất Hóa Học Của Bazơ Và Muối
- Bài 13: Luyện Tập Chương 1 Các Loại Hợp Chất Vô Cơ
- Bài 12: Mối Quan Hệ Giữa Các Loại Hợp Chất Vô Cơ
- Bài 11: Phân Bón Hóa Học
- Bài 10: Một Số Muối Quan Trọng
- Bài 8: Một Số Bazơ Quan Trọng
- Bài 7: Tính Chất Hóa Học Của Bazơ
- Bài 6: Thực Hành Tính Chất Hóa Học Của Oxit Và Axit
- Bài 5: Luyện Tập Tính Chất Hóa Học Của Oxit Và Axit
- Bài 4: Một Số Axit Quan Trọng
- Bài 3: Tính Chất Hóa Học Của Axit
- Bài 2: Một Số Oxit Quan Trọng
- Bài 1: Tính Chất Hóa Học Của Oxit Và Khái Quát Về Sự Phân Loại Oxit
Trả lời